Đề kiểm tra học kì II môn Hóa học 8 - Trường THCS Lý Thường Kiệt (Có đáp án)
Bạn đang xem tài liệu "Đề kiểm tra học kì II môn Hóa học 8 - Trường THCS Lý Thường Kiệt (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề kiểm tra học kì II môn Hóa học 8 - Trường THCS Lý Thường Kiệt (Có đáp án)
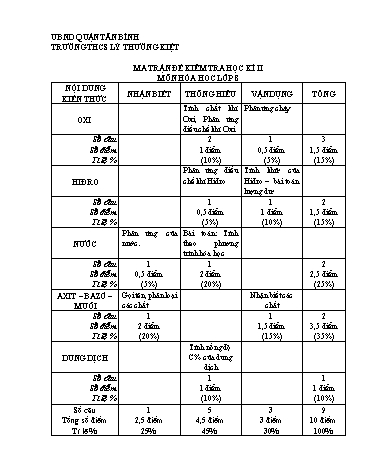
UBND QUẬN TÂN BÌNH TRƯỜNG THCS LÝ THƯỜNG KIỆT MA TRẬN ĐỀ KIỂM TRA HỌC KÌ II MÔN HÓA HỌC LỚP 8 NỘI DUNG NHẬN BIẾT THÔNG HIỂU VẬN DỤNG TỔNG KIẾN THỨC Tính chất khí Phản ứng cháy OXI Oxi, Phản ứng điều chế khí Oxi Số câu 2 1 3 Số điểm 1 điểm 0,5 điểm 1,5 điểm Tỉ lệ % (10%) (5%) (15%) Phản ứng điều Tính khử của HIĐRO chế khí Hiđro Hiđro – bài toán lượng dư Số câu 1 1 2 Số điểm 0,5 điểm 1 điểm 1,5 điểm Tỉ lệ % (5%) (10%) (15%) Phản ứng của Bài toán: Tính NƯỚC nước. theo phương trình hóa học Số câu 1 1 2 Số điểm 0,5 điểm 2 điểm 2,5 điểm Tỉ lệ % (5%) (20%) (25%) AXIT – BAZƠ – Gọi tên, phân loại Nhận biết các MUỐI các chất chất Số câu 1 1 2 Số điểm 2 điểm 1,5 điểm 3,5 điểm Tỉ lệ % (20%) (15%) (35%) Tính nồng độ DUNG DỊCH C% của dung dịch Số câu 1 1 Số điểm 1 điểm 1 điểm Tỉ lệ % (10%) (10%) Số câu 1 5 3 9 Tổng số điểm 2,5 điểm 4,5 điểm 3 điểm 10 điểm Tỉ lệ % 25% 45% 30% 100% UBND QUẬN TÂN BÌNH TRƯỜNG THCS LÝ THƯỜNG KIỆT ĐÁP ÁN HÓA 8 Câu Đáp án Điểm 1 Viết đúng mỗi phương trình hóa học 0, 5 (2,0 điểm) Sai cân bằng -0,25 2 Viết đúng mỗi phương trình hóa học 0, 5 (0,5 điểm) Sai cân bằng -0,25 3 Hoàn thành đúng một ý 0,25 (2,0 điểm) Khối lượng dung dịch thu được: m m m 495,5 4,5 500 (g) 0,5 4 dd H2O NaCl (1 điểm) Nồng độ C% dung dịch thu được: m 4,5 0,5 C% ct 100% 100% 0,9% mdd 500 Dùng quỳ tím để nhận biết các chất 0,25 Quỳ hóa đỏ là nước cốt chanh 0,25 5 do nước cốt chanh là axit 0,25 (1,5 điểm) Quỳ hóa xanh là nước vôi trong 0,25 do nước vôi trong là bazơ 0,25 Quỳ không đổi màu là muối ăn. 0,25 2Na + 2H2O 2NaOH + H2 0,5 0,6 0,6 0,6 0,3 (mol) 0,5 VH 6,72 n 2 0,3 (mol) 0,5 H2 22,4 22,4 mNa nNa .MNa 0,6.23 13,8 (gam) 0,5 to 3H2 Fe2O3 2Fe 3H2O 0,25 6 0,3 0,2 (mol) 0,25 (3 điểm) m 24 m 0,15 (mol) Fe2O3 M 160 So sánh: 0,3 0,15 0,25 tính theo số mol của khí Hiđro 3 1 to 3H2 Fe2O3 2Fe 3H2O 0,3 0,2 (mol) 0,25 mFe nFe.MFe 0,2.56 11,2 (gam) 0,25
File đính kèm:
 de_kiem_tra_hoc_ki_ii_mon_hoa_hoc_8_truong_thcs_ly_thuong_ki.docx
de_kiem_tra_hoc_ki_ii_mon_hoa_hoc_8_truong_thcs_ly_thuong_ki.docx

